Brazil decriminalizes efforts to turn its biota into gold
-
Brazil decriminalizes efforts to turn its biota into gold
Science Magazine, May 22nd 2015
Herton Escobar
SÃO PAULO, BRAZIL—When Carlos Jared tried to ship a jar of dead velvet worms collected in Brazil’s Atlantic Forest to a colleague in Germany in 2006, he had no plans to derive a drug or other product from the creatures. He just wanted to probe the reproductive system of a rare invertebrate that gives birth to live young. But Brazilian authorities denounced him as a “biopirate.”
The evolutionary biologist at the Instituto Butantan in São Paulo had run afoul of a law aiming to clamp down on what Brazil perceived as rampant pillaging of its biological resources. Jared hadn’t filled out all the paperwork required under law MP 2186, so the worms were confiscated. Worse was yet to come. “They dragged my name through the mud. It was a psychological massacre,” he says. It took him 6 years to get another permit for fieldwork, and he is still fighting in court thousands of dollars in fines.
Jared is not the only scientist to run afoul of draconian regulations, sometimes because of nothing more than a clerical oversight. “Biodiversity was deemed so valuable that nobody was allowed to research it anymore,” says Eduardo Pagani, drug development manager at the Brazilian Biosciences National Laboratory in Campinas. “They locked it in a safe and criminalized anyone who tried to work with it.”
But after years of wrangling over how to fix the law, in which officials sought to balance the interests of scientists, the agricultural industry, and biotech firms with those of indigenous populations demanding compensation for traditional knowledge, Brazil President Dilma Rousseff on 20 May signed a law that is raising hopes among scientists. Like its predecessor, the new “biodiversity law” regulates research on “genetic resources”: an all-encompassing term covering everything from genes and proteins to oils and fragrances. It sets rules for sharing benefits with indigenous peoples when R&D leads to a product, such as a drug, shampoo, energy drink, or industrial enzyme, while eliminating bureaucratic hassles and encouraging biodiversity research. Scientists will no longer be “molested” or “bullied” by unreasonable regulation, science minister Aldo Rebelo said on Wednesday while unveiling the law.
The scientific community has greeted the new law with a sigh of relief. “It’s an enormous improvement from what we have now,” says Helena Nader, president of the Brazilian Society for the Advancement of Science in São Paulo. “We hope this will get scientists and industry excited about working with biodiversity again. There is a lot of untapped potential there,” adds Eliana Fontes, a biosafety expert at the Brazilian Agricultural Research Corp. in Brasília and a former president of the Genetic Heritage Management Council (CGEN), the legal body that was created to regulate and enforce MP 2186, now superseded by the biodiversity law.
When MP 2186 came on the books in 2001, its intentions were good. It was passed in response to a contract between the nonprofit company Bio-Amazonia and Novartis that gave the European drug giant exclusive rights to research, patent, and sell products derived from microbes collected in the Brazilian Amazon. (The agreement drew a public outcry and was annulled.) While MP 2186’s goal was to combat biopiracy, its wording cast suspicion on even standard research practices involving life forms. “It was so difficult to get permits that I seriously considered not doing research in Brazil anymore,” says Emilio Bruna, an ecologist at the University of Florida in Gainesville who studies habitat fragmentation in the Amazon and the Cerrado. Two of his students moved their projects to Costa Rica and Ecuador.
Amendments to MP 2186 gradually eased restrictions on basic research. But prospecting for natural compounds remained a daunting challenge. Before starting research, scientists and companies had to get permission from CGEN and sign a benefit-sharing contract with the indigenous group identified with a particular resource. “How can you sign a contract for a product when you don’t know if it’s going to work, or even if it’s going to exist?” asks Paulo Sérgio Beirão, a biochemist at the Federal University of Minas Gerais in Belo Horizonte.
Under the new law, Brazilian scientists need not ask CGEN for permission to do research. All they must do is register their project in a database and document permission from the appropriate indigenous group. Contracts and other legal matters will come into play only if research leads to a product. “A clear distinction is made now between scientific research and technological development for commercial purposes,” says Francine Leal, an environmental lawyer in Curitiba who has consulted on the law. Foreign scientists are prohibited from prospecting for genetic resources in Brazil, unless they are part of a company or institution that strikes a partnership with a Brazilian counterpart.
The law is getting a cool reception from indigenous and other local groups, who believe the rules of access to traditional knowledge and benefit sharing are skewed in favor of companies. “The law moves in the right direction for science and technology,” says Carlos Joly, a plant ecologist at the University of Campinas and a key figure in the regulation of biodiversity research in Brazil, “but there are still major problems with it.” For instance, he says, the law is blurry about the rights of indigenous and local communities to withhold access to traditional knowledge, if they felt an agreement would not benefit them.
Jared, at least, would have fared better under the new law, which abolishes the case-by-case permits for shipments abroad: It only requires noting them in a registry. “The spirit of the law,” Fontes says, “is to trust researchers.” But for Jared, the moment may have passed. He can retrieve his velvet worms from the University of São Paulo’s zoology museum, where they were deposited for safekeeping, but the German colleague he hoped to collaborate with has long since retired.
-
Research paves the way for new drugs against Chagas disease
Agência FAPESP, em 12/05/15
Karina Toledo | Agência FAPESP – Em busca de um novo fármaco para o tratamento da doença de Chagas, pesquisadores do Laboratório Nacional de Biociências (LNBio), em Campinas, têm se dedicado a estudar uma enzima conhecida como glicose-6-fosfato desidrogenase (G6PDH) – essencial para a sobrevivência do parasita Trypanosoma cruzi no organismo humano.
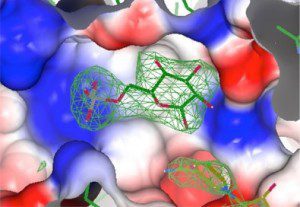
Pesquisadores do LNBio identificam compostos capazes de inibir uma enzima essencial para a sobrevivência do parasita Trypanosoma cruzi. Trabalho ganhou prêmio da Associação Britânica de Cristalografia (divulgação)
Durante o doutorado de Gustavo Fernando Mercaldi, foram identificados ao menos 10 compostos químicos capazes de inibir a ação da enzima e matar o parasita com eficiência comparável à da principal droga hoje usada na clínica: o benzonidazol. A pesquisa contou com Bolsa da FAPESP e foi orientada pelo pesquisador Artur Torres Cordeiro, do LNBio.
Mercaldi tenta agora – durante estágio que realiza na Universidade de Dundee, na Escócia, também com apoio da FAPESP – entender como esses inibidores se ligam à enzima-alvo e desvendar a estrutura tridimensional do complexo formado por essa ligação.
Os primeiros resultados da investigação, conduzida em Dundee sob a supervisão do professor Willian Hunter, já renderam ao brasileiro a indicação para o prêmio David Blow Memorial, concedido anualmente pela Associação Britânica de Cristalografia (BCA, na sigla em inglês).
“Esses compostos capazes de inibir a ação da G6PDH podem servir de inspiração para o desenvolvimento de uma nova droga antichagásica, mas antes é preciso entender de que forma se ligam à enzima. Se conseguirmos desvendar a estrutura tridimensional, poderemos desenhar moléculas com ação potencializada”, explicou Mercaldi.
No T. cruzi, a G6PDH está envolvida no metabolismo de glicose. Dados da literatura científica indicam que, quando a enzima é inibida, o parasita torna-se mais suscetível a morrer em decorrência do estresse oxidativo – condição em que ocorre um aumento nos níveis de espécies reativas de oxigênio que danificam moléculas importantes para o funcionamento das células.
Em estudos anteriores, Cordeiro havia testado um grupo de inibidores pertencentes à classe dos esteroides. Mas, como esse tipo de substância interfere no equilíbrio hormonal humano, poderia desencadear efeitos colaterais indesejáveis. Por esse motivo, durante o doutorado de Mercaldi, o grupo decidiu realizar uma triagem de compostos pertencentes a outras classes químicas.
Por um método conhecido como high throughput screening (triagem automatizada em larga escala), os pesquisadores testaram in vitro – colocando apenas a enzima e o candidato a inibidor para interagir – cerca de 30 mil compostos. Os mais promissores foram testados em culturas do parasita. Foram selecionadas 32 moléculas pertencentes a duas classes químicas: tienopiridinas e quinazolinonas.
“Cerca de 10 dessas moléculas, em especial entre a quinazolinonas, mostraram atividade equivalente à do benzonidazol, que é o composto de referência para o tratamento da doença de Chagas. O caminho até chegar a um novo fármaco ainda será longo, mas comprovamos que é possível matar o parasita ao inibir a enzima G6PDH”, avaliou Mercaldi.
Desvendando a estrutura
O passo seguinte é descrever a estrutura do complexo formado pela enzima e cada um dos inibidores candidatos, bem como determinar em que local da proteína esses compostos se ligam.
“O problema é que a G6PDH é uma proteína difícil de estudar. Há uma certa dificuldade experimental para se obter cristais pelo fato de ela ser muito flexível. Existem algumas regiões que formam alças totalmente móveis e isso resulta em mudanças conformacionais”, explicou Mercaldi.
Graças a um novo método desenvolvido pelo grupo em Dundee, foi possível obter pela primeira vez o cristal da G6PDH de T. cruziem complexo ternário formado pela enzima, seu substrato (glicose-6-fosfato que será oxidado pela enzima para formar o produto da reação) e seu cofator (outra molécula orgânica não proteica capaz de se ligar à enzima).
“Uma das estratégias que usamos foi tirar algumas regiões da proteína para ela ficar mais estável e aumentar a probabilidade de cristalização. Ainda não conseguimos alcançar nossa principal meta, que é obter o cristal da enzima com os inibidores. Mas mostramos pela primeira vez tanto o substrato como o cofator ocupando ao mesmo tempo os seus respectivos sítios de ligação na molécula de G6PDH. Nas pesquisas feitas com enzimas de eucariontes, foi a estrutura com maior resolução já obtida e, assim, um maior nível de detalhes sobre a G6PDH pode ser desvendado”, disse Mercaldi.
Reconhecimento
O pôster descrevendo os resultados foi selecionado durante a BCA Spring Meeting, realizada entre fim de março e início de abril de 2015. Mercaldi será o primeiro pesquisador brasileiro a gravar seu nome no troféu Blue John Crystal.
“O ganhador deve trazer o troféu até a sua instituição de vínculo – no meu caso LNBio e Unicamp no Brasil, bem como a Universidade de Dundee na Escócia – para gravar o nome. No ano seguinte, deve passar o troféu ao novo vencedor”, explicou Mercaldi.
O primeiro grupo a gravar o nome no Blue John Crystal, em 1988, contou com a participação do inglês Richard Charles Garratt, professor da Universidade de São Paulo (USP) e um dos precursores da cristalografia de proteínas no Brasil.
Repercussão: Farol Comunitário; Planeta Universitário; Unifesp; São Carlos; Rede Notícia; Bonde
-
Carlos Américo Pacheco is named new Director General of CNPEM
Communication of CNPEM, 29th April 2015
Available only in PortugueseO Centro Nacional de Pesquisa em Energia e Materiais (CNPEM) realizou nesta quinta-feira (16) a cerimônia de apresentação de seu novo Diretor-Geral, Carlos Américo Pacheco. O evento aconteceu no campus do CNPEM na cidade de Campinas – SP e contou com a presença do Ministro de Estado da Ciência, Tecnologia e Inovação, Aldo Rebelo.
 O Ministro visitou as instalações dos quatro Laboratórios Nacionais do CNPEM e destacou a importância do Centro para a construção da soberania científica e tecnológica do Brasil. Segundo Aldo Rebelo, os temas de pesquisa do CNPEM, como biocombustíveis e doenças negligenciadas, correspondem às demandas mundiais e nacionais. “Aqui se faz ciência voltada às exigências do nosso povo e do Brasil”, afirmou Rebelo.
O Ministro visitou as instalações dos quatro Laboratórios Nacionais do CNPEM e destacou a importância do Centro para a construção da soberania científica e tecnológica do Brasil. Segundo Aldo Rebelo, os temas de pesquisa do CNPEM, como biocombustíveis e doenças negligenciadas, correspondem às demandas mundiais e nacionais. “Aqui se faz ciência voltada às exigências do nosso povo e do Brasil”, afirmou Rebelo.Durante seu discurso de apresentação, Carlos Américo Pacheco reiterou o comprometimento do CNPEM e de seus Laboratórios Nacionais com a produção de novos conhecimentos, o aumento da qualidade de vida dos brasileiros e com a geração de oportunidades econômicas – na fronteira da inovação: “Devemos servir em primeiro lugar ao país, aos seus desafios estratégicos”.
O novo Diretor-Geral também defendeu o modelo de Organização Social, destacando a importância que este modelo de gestão exerce para a produção de melhores resultados. “O Estado brasileiro pode executar políticas públicas com maior impacto e qualidade valendo-se de Organizações Sociais pautadas pelo mérito”, afirmou Pacheco.
Veja a galeria de fotos do evento
Carlos Américo Pacheco foi empossado Diretor-Geral do CNPEM no dia 30 de março deste ano. “O Conselho de Administração do Centro elegeu Pacheco por unanimidade”, lembrou José Ellis Ripper Filho, membro do Conselho de Administração do CNPEM, representante do Diretor do Conselho, Pedro Wongtschowski, na sessão solene. Ex-reitor do Instituto Tecnológico de Aeronáutica (ITA), Pacheco deve cumprir um mandato inicial de três anos.
Jonas Donizette, Prefeito de Campinas; Rogério Cezar de Cerqueira Leite, Presidente Honorário do CNPEM e José Ellis Ripper Filho, representante do Conselho de Administração do CNPEM compuseram a mesa diretora da Sessão Solene, ao lado de Pacheco e do Ministro Aldo Rebelo.
A cerimônia também contou com a presença de convidados e autoridades ligadas diretamente ao desenvolvimento da ciência e da tecnologia no país, como Carlos Henrique de Brito Cruz, Diretor Científico da Fundação de Amparo à Pesquisa (FAPESP); Marco Antonio Raupp, Ex-Ministro de Estado da Ciência, Tecnologia e Inovação; Glaucius Oliva, Ex-Presidente do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq); Prof. Fernando Sakane, Reitor do ITA; Leonel Perondi, Diretor do Instituto Nacional de Pesquisas Espaciais (INPE).
Sobre o CNPEM
O Centro Nacional de Pesquisa em Energia e Materiais (CNPEM) é uma organização social qualificada pelo Ministério da Ciência, Tecnologia e Inovação (MCTI). Localizado em Campinas-SP, possui quatro laboratórios referências mundiais e abertos à comunidade científica e empresarial. O Laboratório Nacional de Luz Síncrotron (LNLS) opera a única fonte de luz Síncrotron da América Latina e está, nesse momento, construindo Sirius, o novo acelerador brasileiro, de terceira geração, para análise dos mais diversos tipos de materiais, orgânicos e inorgânicos; o Laboratório Nacional de Biociências (LNBio) desenvolve pesquisas em áreas de fronteira da biociência, com foco em biotecnologia e descoberta de fármacos; o Laboratório Nacional de Ciência e Tecnologia de Bioetanol (CTBE) investiga novas tecnologias para a produção de etanol celulósico; e o Laboratório Nacional de Nanotecnologia (LNNano) realiza pesquisas com materiais avançados, com grande potencial econômico para o país.
Os quatro Laboratórios têm, ainda, projetos próprios de pesquisa e participam da agenda transversal de investigação coordenada pelo CNPEM, que articula instalações e competências científicas em torno de temas estratégicos.
Discurso na íntegra do diretor-geral do CNPEM, Carlos Américo Pacheco:
Prezados Amigos
Quero saudar todos os colaboradores do CNPEM, pesquisadores, servidores e bolsistas que fazem o sucesso desta instituição.
Quero saudar o Ministro Aldo Rebelo, com a certeza de que vai, apesar das dificuldades, conduzir o Ministério com a visão de que a ciência e a inovação são estratégicas para o desenvolvimento nacional. Saúdo também nosso Prefeito, o Sr. Jonas Donizette, que tem a responsabilidade de liderar este nosso polo tecnológico.
Quero agradecer a presença de todos, do Diretor Científico da FAPESP, o ‘velho’ amigo Dr. Carlos Henrique de Brito Cruz. Quero saudar os amigos do ITA e do DCTA, em nome do reitor, Prof. Fernando Sakane e do Maj. Brig. Wander Golfetto. E agradecer a presença do ex-Ministro Raupp, do Ex-Presidente do CNPq Glaucius Oliva e do diretor do INPE, Dr. Leonel Perondi, em nome de quem cumprimento os dirigentes de C&T, especialmente os colegas aqui de Campinas do CPqD, Eldorado, CTI e do ITAL. E gostaria de agradecer à Unicamp, na pessoa da Prof. Teresa Atvars, pró-reitora de desenvolvimento universitário, pela ampla cooperação e pela minha cessão ao CNPEM.
Queria agradecer ao nosso Conselho de Administração, na figura do Dr. José Ellis Ripper Filho, pela confiança depositada em mim. Queria expressar meu respeito ao Dr. Pedro Wongtschowski, presidente de nosso Conselho e que alia as qualidades de líder empresarial a uma rara clarividência sobre o papel da inovação para nosso futuro.
Deixei o ITA há poucas semanas e assumi o CNPEM com a convicção que os desafios aqui são tão animadores como o reestruturação do ITA e que vamos identificar sinergias entre estes projetos, como revela o fato de muitos iteanos terem contribuído para a história deste Centro, a exemplo desta mesa.
Antes de tudo, quero prestar uma homenagem aos pesquisadores que fizeram deste laboratório algo impar. São muitos, e por isto sintetizo em alguns nomes que estão na sua origem: o Prof. Roberto Lobo, que coordenou as iniciativas precursoras, o Aldo Craievich, primeiro diretor científico do LNLS, o Ricardo Rodrigues, responsável pela engenharia – hoje envolvido com o desafio do Sirius. Um agradecimento especial cabe ao Prof. Rogério Cerqueira Leite, pela sua capacidade de articulação e pela forma como atropela a história e, às vezes, a todos nós também.
Quero prestar um agradecimento especial também ao Prof. Cylon Gonçalves da Silva. O LNLS e o CNPEM tiveram muito bons diretores, como os oito anos do José Antônio Brum e a competente gestão do Dr. Kleber Franchini, no último ano, além da passagem do Michal, do Colli e do Aragão. Mas ninguém está tão identificado com esta instituição e sua transformação em um paradigma de gestão e de capacidade de servir à ciência brasileira como o Cylon – o primeiro defensor do conceito de Organização Social entre nós e, durante anos, a liderança mais obstinada deste projeto.
O que se espera de um Laboratório Nacional é ser relevante para o país. Não se trata de um impacto singular, numa única dimensão. O que fazemos pode ser avaliado em muitas frentes: o que produzimos de conhecimento novo, o que agregamos à qualidade de vida dos brasileiros e o que potencializamos enquanto oportunidades econômicas – na fronteira da inovação.
Os desafios de ampliar o conhecimento estão no nosso DNA. Engenharia e ciência de qualidade, mesmo desinteressada, são a essência deste centro e devem ser nutridas cotidianamente. Isto é decisivo, pois é a paixão pelo conhecimento que atrai talentos e cria a atmosfera que impregna este campus.
Mas nosso mote principal é produzir ciência orientada pelo uso. Pesquisa básica, nada trivial porque distinta do mero desenvolvimento, mas aplicada, voltada aos desafios da vida real. Na caracterização de proteínas, em fármacos, em novos materiais, em alternativas energéticas e em muitas outras frentes. Nosso desafio é o mesmo do país – nosso desejo é idêntico ao da Nação: o desenvolvimento e a soberania.
Este Centro cresceu com naturalidade, embora com polêmicas, a partir das aplicações de suas linhas de luz, de forma a melhor atender seus usuários. Foi assim com a microscopia, com a cristalografia, com a ressonância magnética. Estas infraestruturas complementares se transformaram em novos laboratórios. A reconhecida seriedade do Centro nos levaram a receber também o Laboratório Nacional de Bioetanol.
Uma característica única do CNPEM é reunir competências complementares, em instrumentação, em nanotecnologia, em biologia molecular, em energia, etc. Há poucos Centros desta natureza no mundo e esta é uma vantagem a ser explorada.
Uma segunda singularidade é a capacidade de projetar e construir grandes equipamentos. O Síncrotron não é impressionante, apenas pelo que agregou na capacidade de fazer boa ciência. Foi além, ao ser um projeto ambicioso de engenharia, feito aqui a um custo menor que equipamentos similares. Cercado de muito ceticismo na sua origem, sua construção foi uma ruptura em relação ao passado.
Uma terceira peculiaridade foi se estruturar na forma de uma Organização Social. A ABTLus nasceu antes da Lei das OSs. Várias OSs foram qualificadas desde então. Mas nossa OS, a mais inovadora experiência institucional da ciência brasileira, foi qualificada pela própria Lei, o que é inusitado.
O que nos reserva o futuro? Sem dúvida mais ambição, melhor ciência, maior interdisciplinaridade, mais engenharia, melhor gestão, maior internacionalização, mas especialmente maior impacto na vida nacional.
Como Laboratório Nacional devemos servir em primeiro lugar ao país, aos seus desafios estratégicos. Queremos ser parte das plataformas do conhecimento que precisamos para produzir ciência e tecnologia de qualidade. Queremos ser parte ativa da internacionalização da ciência brasileira, queremos ser parceiros do setor privado na sua tarefa de mudança em direção a atividades de maior valor agregado.
Parte de nosso futuro será norteado pelo Sirius. Um projeto mais ambicioso do que o primeiro Síncrotron. Um projeto de maior risco, por conta das parcerias com empresas na construção de equipamentos e na criação de capacitações tecnológicas que não temos. Um desafio que implica qualificar uma nova comunidade de usuários com as competências necessárias para usar um equipamento de 4ª geração.
Mas nosso maior desafio será reforçar a sinergia entre os Laboratórios que compõe o CNPEM, de modo a mobilizar competências complementares em benefício do país, dos usuários externos e do próprio CNPEM. Explorar esse potencial para produzir ciência e tecnologia de altíssima qualidade, usando e desenvolvendo equipamentos no estado da arte. Ir além do que já fazemos em nossas linhas de luz dedicadas ao estudo de estruturas de proteína e de nanoestruturas, explorando a natureza interdisciplinar do Centro, em aplicações nas áreas da saúde, energia e materiais avançados. Estou convencido de que os diretores dos laboratórios compartilham essa mesma visão.
Este desafio terá de ser acompanhado da consolidação do modelo de Organização Social. Uma OS executa atividades de interesse público através de um Contrato de Gestão. Uma OS é essencialmente uma instituição parceira do Estado, que atua na órbita do direito privado, mas com inúmeros controles: do Conselho de Administração, em que o Estado tem assento, da auditoria interna, da auditoria externa independente e ainda da Comissão de Avaliação. O que difere uma OS é ser avaliada pelos resultados e não procedimentos. Temos procedimentos claros, de compras, de contratações. Mas o central é ter flexibilidade para produzir melhores resultados.
O CNPEM se orgulha de ter produzido resultados esplêndidos. Os próprios órgãos de controle reconhecem isto. Mas é preocupante que a difusão do modelo de OS acirre a tentativa de assemelhá-las à gestão pública tradicional. Sob o condão de conceitos de economicidade e eficiência na alocação dos recursos, volta-se sempre à tentativa de regular o funcionamento das OS pelas normas que regem a administração pública, como infelizmente exemplifica a seção de ontem do Supremo Tribunal Federal.
O exemplo dos laboratórios nacionais norte-americanos deveria nos inspirar. Los Alamos, Argonne, Brookhaven, Oak Ridge são instituições gerenciadas por entidades privadas sem fins lucrativos. Hoje são 39 grandes centros de P&D que geram resultados expressivos e asseguram a retenção de recursos humanos qualificados.
Caro Ministro, nosso esforço aqui foi, é e será mostrar que o Estado brasileiro pode executar políticas públicas com maior impacto e qualidade valendo-se de Organizações Sociais pautadas pelo mérito. Somos e queremos ser exemplares e faremos tudo para isto, inclusive aprimorando o modelo de gestão. Como escreveu o Marechal Casimiro Montenegro, o idealizador do ITA e do CTA, em documento dos anos sessenta: “Ensino e pesquisa, em alto nível e com adequada produtividade, são comprovadamente incompatíveis com a estruturação da administração pública comum”.
Precisamos de ajuda para evitar retrocessos. E precisamos de sua ajuda para atravessarmos este período de ajuste fiscal necessário, mas difícil. Esta é uma preocupação enorme de todos nós, mas não é momento, nem o local para aprofundarmos esta discussão.
Só posso dizer que darei o melhor de mim para corresponder às expectativas de minha indicação para a Direção Geral. Conto com o apoio da equipe da Casa – todos aqueles que, diariamente, aqui trabalham muito motivados por ideais de produzir ciência e tecnologia de qualidade.
É uma empreitada que vale muito a pena, pelo que pode contribuir ao país.
Muito Obrigado.
-
LNBio represents Brazil in international consortium
Portal do MCTI, 9th April 2015
Available only in PortugueseBrasil sedia encontro de consórcio europeu para desenvolvimento de fármacos
Representantes de 13 instituições de pesquisa estão em Campinas (SP) para debater o andamento do projeto New Medicines for Trypanosomatidic Infections (NMTryI), um consórcio internacional para o desenvolvimento de fármacos contra a doença de Chagas, leishmaniose e doença do sono, também conhecida como tripanossomíase humana africana. O encontro acontece no auditório do Centro Nacional de Pesquisas em Energia e Materiais (CNPEM), uma organização social supervisionada pelo Ministério da Ciência, Tecnologia e Inovação.
Nesta sexta-feira (10), pesquisadores divulgarão ao público o modelo de consórcio multinacional e as oportunidades de interação entre grupos do Brasil e da Europa. O simpósio “Building International Consortia on parasitic diseases: the NMtrypl experience” também será realizado no CNPEM. “Esse é um evento importante para apresentar uma forma diferente de trabalhar”, explica o coordenador da parte brasileira no projeto NMTryI, Lúcio Freitas-Junior, que também é pesquisador do Laboratório Nacional de Biociências (LNBio). “O Brasil tem um grande número de grupos de pesquisa de excelência na área e que poderão ajudar nos estudos.”
Com orçamento de 7,6 milhões de euros, o projeto começou em 2014 e se estende até 2017. A iniciativa é financiada pela União Europeia, por meio do Programa FP7. O consórcio europeu reúne grupos com diferentes tecnologias e especialidades para maximizar a eficiência e reduzir os custos no processo de inovação em fármacos para doenças negligenciadas.
De acordo com o 2º Relatório da OMS sobre Doenças Tropicais Negligenciadas, 1 bilhão de pessoas estão em risco ou são afetadas por doenças tropicais negligenciadas. Lucio Freitas-Junior alerta que muitas dessas enfermidades estão presentes em todos os países devido aos movimentos de migração globais. “Essas doenças não precisam de passaporte e visto para chegar aos países. Desenvolver fármacos para elas é, mais que uma oportunidade de negócio e crescimento tecnológico, uma maneira de ajudar as populações menos favorecidas”, disse.
Além do LNBio pelo lado brasileiro, participam do consórcio instituições da Alemanha, Portugal, Itália, Sudão, Reino Unido, Grécia, Espanha e Bélgica.
Para mais informações sobre o simpósio, clique aqui.
Sobre o LNBio
O LNBio é responsável pela triagem de moléculas capazes de matar os parasitas da família Trypanosomatidae. “Foram enviadas [ao LNBio] cerca de 15 mil frações isoladas provenientes de fungos. Ao todo, já analisamos cerca de 50 mil pontos de triagem”, afirmou Lúcio Freitas-Júnior. “O resultado alimentou diferentes grupos que darão seguimento aos estudos baseados nos nossos dados.”
O pesquisador explica que o trabalho do grupo de Biologia Química e Plataforma de Triagem do LNBio é tentar simular em laboratório o que acontece no sistema humano. “Colocamos células humanas em uma placa e depois as infectamos com um dos parasitas. Tentamos tratar as células contaminadas com as drogas que estamos testando, sendo o objetivo final matar o parasita sem danificar a célula”, resume Freitas-Junior, que também é coordenador do grupo. “Nosso desafio é ter um sistema relevante para seres humanos em uma placa.”
A técnica, conhecida como Triagem Fenotípica ou Triagem Celular, oferece com uma das vantagens a redução de falsos positivos. “Tem que haver uma correlação entre o que descobrimos no começo com o que será testado alguns anos depois. Estamos preocupados em obter resultados. Descobrir um fármaco é uma tarefa complicada e cara, e, justamente por isso, você precisa reduzir ao máximo o número de falsos positivos.”
O LNBio é um dos quatro laboratórios associados ao CNPEM. A organização social conta ainda com os laboratórios nacionais de Luz Síncroton (LNLS), de Nanotecnologia (LNNano) e de Ciência e Tecnologia do Bioetanol (CTBE).
-
A developmental regulator of bacterial division
Agência FAPESP, 8th April 2015
Karina Toledo
Available only in PortugueseEstudo da USP desvenda mecanismo de inibição da divisão bacteriana
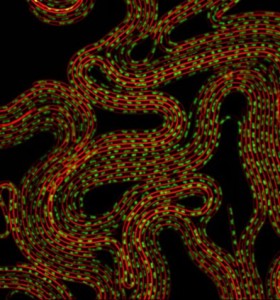
Células de Bacillus subtilis forçadas a produzir a proteína MciZ não conseguem se dividir e se transformam em longos filamentos multinucleados. A cor vermelha representa a membrana celular e a verde, o DNA bacteriano (divulgação)
Em um artigo divulgado segunda-feira (06/4) na revista Proceedings of the National Academy of Sciences, pesquisadores do Instituto de Química da Universidade de São Paulo (IQ-USP) descreveram em detalhes o mecanismo pelo qual uma proteína chamada MciZ inibe o processo de divisão bacteriana.
A investigação foi conduzida no âmbito do projeto “Smolbnet 2.0: combinando genética e RMN para dissecar interações proteína-proteína fundamentais para o funcionamento do complexo de divisão bacteriana”, coordenado por Frederico José Gueiros Filho e apoiado pela FAPESP.
“O estudo de proteínas que naturalmente inibem a divisão de bactérias, além de permitir que compreendamos como o processo de divisão é regulado pela célula, pode inspirar o desenvolvimento de inibidores sintéticos e abrir caminho para uma nova classe de antibióticos. As proteínas que compõem o aparato de divisão celular são um alvo terapêutico atraente que ainda não é atacado pelos antibióticos disponíveis comercialmente”, afirmou Gueiros à Agência FAPESP.
De acordo com o pesquisador, existem cerca de 20 proteínas especializadas em executar a divisão das bactérias, sendo a FtsZ a mais importante de todas. Para estudar a interação entre essas proteínas, o grupo do IQ-USP usa como modelo a espécie Bacillus subtilis, que costuma habitar o solo e não causa doença em humanos.
“É um organismo muito fácil de ser estudado e, portanto, serve de exemplo para outros. Como o mecanismo de divisão é semelhante em todas as bactérias – sempre dependente de FtsZ –, o que aprendemos com Bacillus subtilis é aplicável a muitas outras espécies, inclusive as patogênicas”, disse.
Quando tem início o processo de reprodução bacteriana, explicou o pesquisador, as moléculas de FtsZ se entrelaçam umas às outras formando filamentos. Esses filamentos se agrupam em uma espécie de anel contrátil, que marca o local onde ocorrerá a divisão.
Ao formar essa “cintura” na parte interna, a FtsZ atrai outras proteínas de divisão para o anel, que alteram a parede externa da bactéria. No momento da divisão, a parede bacteriana para de se expandir no comprimento e passa a crescer para dentro, formando um septo que separa a bactéria em duas células-filhas.
Mas para evitar que a divisão ocorra na hora ou local inadequados, existem no interior da célula proteínas que funcionam como inibidores naturais, capazes de impedir a formação do anel contrátil. Entre as mais importantes estão a MciZ e a MinC – alvos do projeto coordenado por Gueiros.
“Nós já sabíamos que a MciZ se ligava à FtsZ e isso de alguma maneira impedia a formação do anel contrátil. Mas para entender como isso ocorre em nível molecular recorremos a técnicas de biologia estrutural”, contou o pesquisador.
Por meio de um método conhecido como cristalografia de raios X, os pesquisadores desvendaram a estrutura tridimensional do complexo formado pelas proteínas FtsZ e MciZ. Já com a ajuda da ressonância magnética nuclear (RMN), os cientistas estudaram a estrutura tridimensional da MciZ isolada.
O trabalho contou com a colaboração das pesquisadoras Ana Carolina Zeri, do Laboratório Nacional de Biociências (LNBio), e Andrea Dessen, que atua no Instituto de Biologia Estrutural (IBS) em Grenoble, na França, e também no LNBio por meio do programa São Paulo Excellence Chair (SPEC), da FAPESP.
Alvo terapêutico
“Quando desvendamos a estrutura de complexos proteicos, podemos descobrir que porções de cada uma das proteínas estão se tocando e, dessa forma, deduzir o mecanismo pelo qual uma está inibindo a outra. O sítio onde ocorre a interação é um alvo para o desenvolvimento de fármacos”, disse Gueiros.
Uma série de experimentos bioquímicos in vitro foi realizada para complementar o entendimento da interação entre as duas proteínas. Os cientistas observaram que a molécula de MciZ se liga na ponta dos filamentos, exatamente onde deveria entrar uma outra molécula de FtsZ. Dessa forma, o filamento para de crescer.
“Na ausência de MciZ, o filamento composto de moléculas de FtsZ cresce até atingir cerca de 40 subunidades e então ocorre a formação do anel contrátil. Mas basta uma pequena quantidade de MciZ – algo na proporção de 1 para 20 – para reduzir o tamanho do filamento pela metade e tornar impossível a formação do anel e a divisão celular”, explicou Gueiros.
Segundo o pesquisador, trata-se de um mecanismo de inibição poderoso, pois não é necessário que a MciZ se ligue a cada uma das subunidades de FtsZ. “Isso deve ser levado em conta na hora de desenhar inibidores sintéticos, pois permite que o fármaco atue em concentrações mais baixas”, avaliou.
Em um trabalho anterior divulgado na revista PLoS One em 2013, o grupo investigou mutações na cadeia de aminoácidos que formam a proteína FtsZ e a impedem de se ligar à MinC, também inibidora da divisão.
“O mecanismo de atuação nesse caso é diferente, pois a MinC não se liga na ponta do filamento e sim na lateral da molécula de FtsZ. Ainda assim, ela impede a formação do anel contrátil”, contou Gueiros.
Apesar das potenciais implicações práticas dos resultados obtidos, a principal motivação do grupo de Gueiros é compreender os mecanismos celulares em seu nível mais fundamental.
“A boa pesquisa básica, além de avançar a nossa compreensão da natureza, tem sido a principal fonte das descobertas que alimentam a inovação e a tecnologia”, disse o pesquisador.
O artigo FtsZ filament capping by MciZ, a developmental regulator of bacterial division (doi: 10.1073/pnas.1414242112) pode ser lido em www.pnas.org/content/early/2015/04/02/1414242112.abstract” target=.
-
Alternatives to in vivo animal testing
Agência FAPESP, 6th April 2015
Diego Freire
Available only in PortugueseTestes em animais são reduzidos com novos ensaios in vitro e simulações
Impulsionada pela opinião pública e pelo desenvolvimento científico e tecnológico da toxicologia, que estuda os efeitos de substâncias químicas sobre os organismos, a busca por métodos alternativos aos testes de laboratório em animais já apresenta resultados: simulações de interações moleculares em computador e novas tecnologias para ensaios in vitro minimizam o uso de cobaias e apontam para um futuro livre de testes in vivo.
Esforços de instituições nacionais e estrangeiras nesse sentido foram apresentados no workshop Challenges and perspectives in research on alternatives to animal testing, realizado na FAPESP no dia 31 de março. Para os especialistas participantes, é preciso desenvolver e adotar alternativas aos testes em animais para a redução do uso de cobaias e dos riscos para o próprio ser humano, pois, dadas as particularidades das espécies, os resultados dos experimentos não são suficientemente eficazes.
“Os testes em animais vêm sendo usados há muitas décadas, mas nunca refletiram de maneira adequada os efeitos das substâncias testadas quando aplicadas ao organismo do ser humano. É preciso avançar por questões éticas e também científicas, incorporando novas tecnologias e abordagens à toxicologia”, disse Thomas Hartung, do Center for Alternatives to Animal Testing do Johns Hopkins University Hospital, em Maryland, nos Estados Unidos, à Agência FAPESP.
No workshop, Hartung tratou da implementação do princípio dos três Rs da experimentação animal, elaborados em 1959 pelos ingleses William Russel e Rex Burch: refinamento, redução e substituição (replacement, em inglês), que consistem na diminuição da quantidade de animais utilizados na pesquisa, na melhora na condução dos estudos para minimizar o sofrimento das cobaias e no desenvolvimento de sistemas experimentais que reproduzam as condições dos organismos, dispensando modelos vivos.
“A ideia é utilizar novos métodos que, em vez de comprometer a qualidade do trabalho, ampliem a confiança nos resultados. O refinamento, por exemplo, ao aprimorar os procedimentos para minimizar a dor e o estresse das cobaias, tem impacto também nos resultados por controlar alterações psicológicas nos animais, que aumentam a variabilidade experimental dos resultados”, afirmou.
Maria José Soares Mendes Giannini, pró-reitora de Pesquisa da Universidade Estadual Paulista (Unesp) e coordenadora do workshop, enfatizou que a busca por alternativas aos testes em animais é condição para o avanço da ciência.
“Além das razões de ordem ética, que estão no cerne da busca por alternativas aos testes in vivo e de toda a demanda para diminuir e evitar o sofrimento dos animais, é urgente a questão do avanço científico. Os modelos animais são comprovadamente limitados, não permitem obter respostas de qualidade suficientemente boas”, afirmou Giannini, que também é membro do Conselho Superior da FAPESP.
“Novos medicamentos muito avançados, como os imunobiológicos, se aplicados em um modelo animal não provocarão reações comparáveis à maneira como nós, humanos, reagiríamos. Os testes toxicológicos precisam acompanhar esse desenvolvimento, avançando para além dos modelos animais”, disse.
Órgãos em chips
Durante o workshop, Wagner Quintilio, do Instituto Butantan, apresentou uma série de resultados de estudos empregando métodos in vitro para substituir o uso de animais no desenvolvimento e controle de qualidade de imunobiológicos produzidos na instituição.
Para Chantra Eskes, da European Society of Toxicol in vitro, a humanidade caminha para dispensar o uso de animais em testes de laboratório especialmente por conta da evolução dos testes in vitro.
“A humanidade vive uma grande revolução científica com a possibilidade de retornar células ao seu estado inicial e, a partir delas, produzir tecidos e órgãos para aplicar testes com substâncias tóxicas nas células do próprio paciente. Com o conhecimento crescente do genoma, do transcriptoma e do proteoma humanos, o caminho para a substituição dos testes in vivo por ensaios in vitro mais avançados está traçado”, disse Eskes.
Nesse sentido, Silvya Maria-Engler, da Universidade de São Paulo (USP), apresentou resultados promissores sobre o modelo tridimensional de epiderme desenvolvido no Brasil.
Empregando células primárias de pele humana, o modelo tem sido adotado em estudos de irritação e corrosão cutânea em substituição aos ensaios em animais e na avaliação da eficácia de moléculas candidatas a fármacos antimelanoma, além de estudos de doenças de pele e outras pesquisas.
Essa revolução, agregada a novas tecnologias aplicadas aos testes in vitro, compensa a deficiência dos modelos animais na similaridade com o organismo humano, disse Eduardo Pagani, do Laboratório Nacional de Biociência (LNBio).
“Além de culturas celulares, podemos ter tecidos, que são grupos de células organizadas e que podem ser cultivados em dimensões mais complexas, buscando-se uma maior correspondência com a morfologia normal dos tecidos humanos”, explicou Pagani, referindo-se às culturas organotípicas, que combinam diferentes tipos celulares.
O pesquisador apresentou, em sua palestra, o conceito de organs-on-a-chip, tecnologia em fase inicial de desenvolvimento em algumas instituições estrangeiras que utiliza células-tronco para fazer crescer órgãos humanos integrados a microchips capazes de reproduzir o funcionamento de órgãos vivos, como o pulmão e o coração.
De acordo com Pagani, o LNBio, junto com a Rede Nacional de Métodos Alternativos (Renama), está buscando associação com grupos que possuem a tecnologia para trabalhar em parceria no desenvolvimento de testes de avaliações de toxicidade em organs-on-a-chip.
Testes in silico
Outra importante frente de desenvolvimento de alternativas a testes em animais é a simulação em computador, chamada de teste in silico.
“Nos testes computacionais, o que se faz é acessar bases de dados de drogas já testadas e buscar semelhanças com as drogas novas, efeitos semelhantes de toxicidade e absorção farmacocinética ou até mesmo eficácia para determinadas indicações. Trata-se de predições teóricas feitas por comparações da molécula nova com outras já testadas”, disse Pagani.
No entanto, o pesquisador explica que “os testes in silico ainda não eliminam a necessidade de experimentações com animais, mas reduzem a quantidade de substâncias a serem testadas in vivo”.
Raymond Tice, do National Institute of Environmental Health Science dos Estados Unidos, apresentou no workshop os resultados do programa norte-americano Toxicologia do Século 21 (Tox 21), que mostra os efeitos de diversas substâncias químicas sobre diferentes vias de sinalização celular em modelos robóticos de alto desempenho (high throughput screening). A iniciativa apresenta uma nova visão da avaliação de risco, diferente da toxicologia tradicional, para caracterizar as vias de toxicidade e doença.
Foram apresentados ainda, nas palestras de Cláudia Vianna Maurer Morelli, da Universidade Estadual de Campinas (Unicamp), e Giannini, modelos alternativos ao uso de mamíferos, como o peixe-zebra, popularmente conhecido como paulistinha, e o inseto Galleria mellonella, a traça da cera.
Regulação
A comunidade científica internacional adota uma série de métodos alternativos que têm reduzido e substituído o uso de animais em testes toxicológicos. Os parâmetros variam entre os países. Na União Europeia, por exemplo, desde 2003 nenhum cosmético pode ser vendido se o produto final ou qualquer um de seus ingredientes tiver sido testado em animais – a não ser que não haja métodos alternativos validados.
“O Brasil caminha para acompanhar o que está acontecendo em países como os Estados Unidos e os da Europa, com importantes avanços nessas áreas, mas é preciso acelerar e avançar mais”, disse Giannini.
Ano passado, em resposta a solicitação do Conselho Nacional de Controle de Experimentação Animal (Concea), a Agência Nacional de Vigilância Sanitária (Anvisa) deliberou pela aceitação de 17 métodos alternativos ao uso de animais validados internacionalmente.
“São testes in vitro que medem o potencial de irritação e corrosão da pele e dos olhos, a absorção cutânea e outras interações. Os laboratórios do Brasil têm até 2019 para adotar os 17 métodos validados que substituem ou reduzem o uso de animais em testes toxicológicos”, disse José Mauro Granjeiro, coordenador do Concea.
Em março, o órgão abriu consulta pública para sugestões que aprimorem o capítulo sobre primatas não humanos mantidos em cativeiro do Guia Brasileiro de Produção e Utilização de Animais para Atividades de Ensino ou Pesquisa Científica. O texto compila informações necessárias para garantir boas condições de produção, manutenção ou utilização dos animais, com foco no bem-estar das espécies e na qualidade das pesquisas e dos procedimentos didáticos.
O workshop contou ainda com palestra de Joel Majerowicz, da Diretoria de Gestão Institucional da Anvisa, que apresentou a estrutura da instituição e demonstrou o interesse em políticas para adoção de novas abordagens de avaliação toxicológica.
Apresentações feitas pelos pesquisadores no workshop estão disponíveis em: www.fapesp.br/9310.
-
LNBio represents Brazil in International Consortium
Communication of LNBio, 9th March 2015
Click here to dowload the English Version
Consórcio internacional para o desenvolvimento de novos fármacos contra Doença de Chagas, Leishmaniose e Doença do Sono se reúne pela primeira vez no Brasil. Representantes de institutos de pesquisa e empresas de biotecnologia de nove países estarão em Campinas – SP para discutir o andamento do Projeto NMTryI, sigla para “New Medicines for Trypanosomatidic Infections”, uma iniciativa financiada pela União Europeia, por meio do Programa FP7 (www.nmtrypi.eu). Os pesquisadores também participarão de um simpósio, aberto ao público, sobre oportunidades de parcerias entre instituições brasileiras e europeias. Os eventos acontecerão entre os dias 8 e 10 de abril no campus do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM).
Com orçamento de EUR 7,6 milhões e duração de três anos, o Projeto NMTrypI tem como principal objetivo otimizar moléculas com ação anti-tripanossoma, a fim de garantir medicamentos mais eficientes contra Doença de Chagas, Leishmaniose e Doença do Sono, também conhecida como Tripanossomíase Humana Africana. Essas doenças atingem principalmente populações de países em desenvolvimento e seus tratamentos são baseados em medicamentos antigos, os quais apresentam problemas de resistência e toxicidade. Para o desenvolvimento de novos fármacos, o consórcio investe em uma abordagem interdisciplinar e na reunião de competências de entidades da Itália, Alemanha, Portugal, Inglaterra, Grécia, Espanha, Bélgica, Sudão e Brasil.
O País é representado nesta iniciativa pelo Laboratório Nacional de Biociências (LNBio), integrante do CNPEM. O LNBio é responsável pela triagem das moléculas candidatas a fármacos, por meio de high throughput screening (HTS) – técnica automatizada utilizada para identificação de compostos que interferem nos mecanismos das doenças. “Estamos testando aproximadamente 15 mil substâncias em ensaios celulares para doença de Chagas, leishmaniose e Doença do Sono. Ao todo, realizaremos mais de 50 mil pontos de triagem”, detalha Carolina Borsoi Moraes, pesquisadora do LNBio, especialista em triagem para doenças negligenciadas.
“O Projeto NMTrypI alavancará um montante de mais de EUR 365 mil à Plataforma de Biologia Química e Triagem do LNBio, um investimento que beneficiará o processo nacional de descoberta e desenvolvimento de fármacos, por meio do treinamento de pessoal e aquisição de equipamentos”, afirma Lucio Freitas-Junior, pesquisador do LNBio, responsável pela participação brasileira no consórcio.
Simpósio: Oportunidades de Interação
Para disseminar o modelo de consórcio multinacional e apresentar oportunidades de interação entre grupos do Brasil e da Europa, principalmente na área de doenças negligenciadas, será realizado o simpósio: “Building International Consortia on parasitic diseases: the NMtrypl experience”, no dia 10 de abril, no Campus do CNPEM. O evento é aberto à comunidade científica e as inscrições são gratuitas. “A Comissão Europeia apoia este tipo de parceria para promover a aproximação entre diferentes grupos de pesquisa, estimular colaborações científicas e, assim, favorecer o avanço da ciência e da economia internacional” explica Maria Paola Costi, Coordenadora do Projeto NMTrypI e pesquisadora da Universidade de Módena e Reggio Emília na Itália. Detalhes sobre o simpósio estão disponíveis em: http://pages.cnpem.br/nmtrypi/
-
Opportunity: Scientific Initiation
Communication of LNBio, 30th January 2015
Available only in Portuguese
Oportunidade: Iniciação Científica
O Laboratório Nacional de Biociências (LNBio) divulga oportunidade de iniciação científica para o projeto: “Structural Studies of the Interaction of Normal and Pathological RAR and TR with Corepressors”, aprovado pelo PROGRAMA CIÊNCIA SEM FRONTEIRAS – FELLOWSHIP IN BRAZIL -YOUNG TALENT ATTRACTION – BJT – CALL FOR PROJECTS MEC / MCTI / CAPES / CNPq / FAPs No. 02/2014 e com bolsa concedida pelo CNPq.
O projeto será conduzido por um pesquisador visitante, que virá do CNRS/França para o Brasil, e supervisionado pela Dra. Ana Carolina Migliorini Figueira, pesquisadora do LNBio. O início das atividades será em agosto de 2015, com duração de três anos.
Interessados nessa oportunidade devem estar cursando a graduação em ciências biológica, ciências moleculares, farmácia, bioquímica, química, engenharia química, ou áreas afins e ter domínio da língua inglesa. Os candidatos devem encaminhar CV, histórico escolar e uma carta de recomendação para o email rb.mepncnull@acinumocoibnl, até o dia 31 de março.
O estudante selecionado trabalhará com técnicas de biologia estrutural de proteínas, utilizando técnicas biofísicas, como cristalografia, SAXS e espectroscopia, além de trabalhar com biologia molecular, com expressão e purificação de proteínas.
-
Sao Paulo School of Advanced Science Neglected Diseases on Drug Discovery focus on Kinetoplastids (SPSAS-ND3)
Applications for the Sao Paulo School of Advanced Science Neglected Diseases Drug Discovery – focus on Kinetoplastids (SPSAS-ND3) is open until February 18th 2015. The event is promoted by LNBio (The Brazilian Biosciences National Laboratory) and will be hosted in the Brazilian Center for Research in Energy and Materials (CNPEM) Campus – Campinas-SP, Brazil from 14th to 24th June, 2015. The SPSAS-ND3 is funded by FAPESP (Sao Paulo Research Foundation) and aims to support courses in advanced themes in science and technology, contributing to the formation of young researchers and attraction of both national and international scientific talents to Sao Paulo state.
The SPSAS-ND3 will focus on multidisciplinary aspects of drug discovery applied to Chagas disease, human African tripanosomiasis and leishmaniasis, introducing students to the basics of drug discovery science and cutting-edge research on the field. The course is structured in both lectures and practical activities covering high throughput and high content screening, structural biology and virtual screening, screening data analysis, medicinal chemistry, lead optimization, in vitro and in vivo ADME, and in vivo models for pharmacokinetics and efficacy studies.
The School will comprise practical and theoretical activities, ministered by a panel of world-class drug discovery scientists and parasitology experts, originating from both Pharma and Academia, and combining academic excellence with the product-oriented pragmatism of the Pharma and Biotech companies.
The event does not have a registration fee, however the attendance is limited and application is required. For more information, please, visit the SPSAS-ND3 website: http://pages.cnpem.br/drugdiscovery-kinetoplastids/.
-
LNBio signs collaboration research agreement with Phytobios
Communication of LNBio, 9th December 2014
Available only in Portuguese
Inovação em parceria com a biodiversidade nacional
LNBio e Phytobios firmam acordo para identificar moléculas bioativas em extratos vegetais
O Laboratório Nacional de Biociências (LNBio), integrante do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), firmou parceria com a Phytobios, empresa voltada à inovação a partir da biodiversidade brasileira. O acordo tem como principal objetivo identificar moléculas bioativas em extratos vegetais extraídos de biomas brasileiros. Amostras de plantas da Mata Atlântica de São Paulo e da Caatinga do Piauí serão as primeiras a serem avaliadas.
Os primeiros ensaios buscarão substâncias com ação antidepressiva. Em seguida, serão realizados testes para identificação de compostos contra infecções bacterianas, câncer, hipertrofia cardíaca, doença de Chagas, doença do sono e leishmaniose.
“A parceria com o LNBio é uma iniciativa de valorização da biodiversidade brasileira. Vamos identificar compostos com potencial valor de mercado em amostras coletadas com autorização dos órgãos competentes, por meio de técnicas que garantem a conservação das espécies” afirma Cristina Ropke, Diretora Executiva da Phytobios.
De acordo com o contrato firmado, a Phytobios disponibilizará centenas extratos brutos ao LNBio. No Laboratório, esses extratos serão divididos em frações, cada uma contendo cerca de 10-20 substâncias químicas diferentes. “O fracionamento facilita a identificação de moléculas bioativas e permite um rígido controle de qualidade. Ao final deste processo, teremos cerca de 2000 frações organizadas em uma biblioteca de produtos naturais apropriadas para triagem biológica de alto desempenho, high throughput screening (HTS), e prontas para serem analisadas”, explica Daniela Trivella, pesquisadora do LNBio.
O LNBio fará a triagem das frações por meio de HTS, técnica comum ao processo de descoberta de fármacos. O HTS é um método automatizado que testa rapidamente milhares de substâncias químicas em ensaios biológicos preditivos de eficácia clínica. Os resultados destes testes permitem a identificação de compostos que interferem nos mecanismos das doenças, em vias metabólicas-chave ou que interagem com alvos moleculares específicos. Substâncias avaliadas como promissoras em ensaios de HTS seguem para ensaios subsequentes, que tem por objetivo confirmar os dados obtidos nas primeiras triagens e compreender os detalhes da interação do composto selecionado com as moléculas biológicas. Trata-se do ponto de partida para a descoberta e aprimoramento de compostos com potencial terapêutico.
“Esta parceria é muito promissora porque reúne competências complementares. Temos a experiência da Phytobios com coleta e preparo de extratos vegetais a partir de espécies da biodiversidade brasileira e a expertise do LNBio na montagem de bibliotecas de produtos naturais e na realização dos ensaios biológicos e ensaios subsequentes. A colaboração promoverá a pesquisa e o desenvolvimento de fitoterápicos nacionais, uma classe de medicamentos bastante promissora”, conclui Eduardo Pagani, Gerente de Inovação do LNBio.
Sobre o LNBio
O Laboratório Nacional de Biociências (LNBio) integra o Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), uma organização social qualificada pelo Ministério da Ciência, Tecnologia e Inovação (MCTI). O LNBio dedica-se à pesquisa e inovação nas áreas de biotecnologia e à descoberta e desenvolvimento de fármacos e possui instalações abertas às comunidades científicas e empresariais. O Laboratório concentra competências, equipamentos de última geração e um time de pesquisadores de classe mundial voltados à realização de estudos multidisciplinares nas áreas de biologia estrutural, proteômica, genômica, metabolômica, bioensaios, desenvolvimento de organismos geneticamente modificados, dentre outros.
Sobre a Phytobios
A Phytobios é uma empresa brasileira voltada para desenvolvimento e comercialização de tecnologias baseadas em biodiversidade por meio de pesquisa, licenciamento, propriedade intelectual, apoio regulatório e gestão de inovação. A empresa atua no desenvolvimento de tecnologias para a área farmacêutica, cosmética, alimentos e tecnologias naturais, realizando desde a fase de pesquisa até o desenvolvimento de protótipos utilizando produtos/processos com uso sustentável, oriundos da biodiversidade e/ou rotas biotecnológicas, sempre respeitando a legislação de acesso ao patrimônio genético. Em janeiro de 2014 foi inaugurada a primeira filial da Phytobios. A filial conta com o Laboratório de Inovação em Produtos Naturais (LIPRON), localizado no Município de Parnaíba, Litoral do Estado do Piauí e uma área especialmente dedicada à experimentação agrícola com as melhores práticas de agroecologia. O LIPRON é um laboratório voltado a obtenção de extratos/ativos de alto valor para Pesquisa & Desenvolvimento, assim como bioprospecção a partir da biodiversidade para as mais diversas finalidades ligadas a tecnologias naturais e biotecnologia. A Phytobios dentro deste contexto também contribui de forma efetiva na formação de recursos humanos ligados a projetos de inovação em programas nacionais e internacionais como FINEP subvenção, Inova Talentos IEL/CNPq e RHAE/CNPq por acreditar que a capacidade técnica com excelência constitui o verdadeiro alicerce do desenvolvimento com sustentabilidade.


